MLZ ist eine Kooperation aus:
 > Technische Universität München
> Technische Universität München > Helmholtz-Zentrum Hereon
> Helmholtz-Zentrum Hereon
 > Forschungszentrum Jülich
> Forschungszentrum Jülich
MLZ ist Mitglied in:
 > LENS
> LENS > ERF-AISBL
> ERF-AISBL
MLZ in den sozialen Medien:

MLZ
Lichtenbergstr.1
85748 Garching
08.01.2018
Struktur von Membranproteinen mit Neutronen aufklären
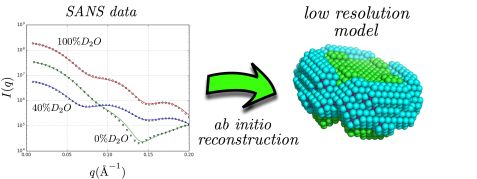
Ergebnisse der Neutronenstreuung an Komplexen des Membranproteins Aquaporin-0 und dem Lösungsmittel n-Dodecyl β-D-Maltoside (links). Rechts ist die Rekonstruktion des Aussehens mit der neuen Methode zu sehen. © Forschungszentrum Jülich
Membranproteine erfüllen wichtige biologische Funktionen. Zum Beispiel bilden sie Pforten für die Einfuhr von Nähr- und Botenstoffen ins Zellinnere oder für die Abgabe von Stoffwechselprodukten. Die Wirksamkeit von Medikamente beruht oft auf Membranproteinen.
Um die Funktion solcher Proteine zu verstehen, ist es wichtig, ihren Aufbau im Detail zu kennen. Die üblichen Methoden zur Strukturaufklärung von Proteinen funktionieren jedoch bei Membranproteinen oft nicht. Wissenschaftler des Jülich Centre for Neutron Science zeigen nun, dass sich der Aufbau von Membranproteinen mittels Neutronen mit einer Auflösung von 1-2 Nanometern untersuchen lässt.
Text: A. Wenzik / JCNS
Originalveröffentlichung:
A. Koutsioubas
Low Resolution Structure Determination of Detergent Solubilised Membrane Proteins from Small Angle Scattering Data
Biophys.J. 2017;113(11):2373-2382, DOI: 10.1016/j.bpj.2017.10.003
Über Open Access bis Ende Januar 2018 verfügbar
MLZ ist eine Kooperation aus:
 > Technische Universität München
> Technische Universität München > Helmholtz-Zentrum Hereon
> Helmholtz-Zentrum Hereon
 > Forschungszentrum Jülich
> Forschungszentrum Jülich
MLZ ist Mitglied in:
 > LENS
> LENS > ERF-AISBL
> ERF-AISBL
MLZ in den sozialen Medien:


